Effekt inntil 52 uker ved ulcerøs kolitt
Studiedesign GEMINI I1,2
Induksjonsbehandling
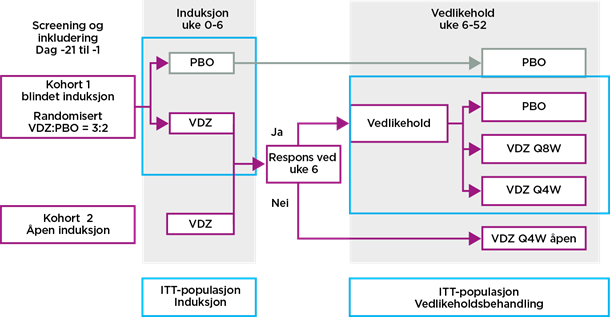
I Gemini I ble pasienter randomiserte til å få blindet induksjonsbehandling med Entyvio® eller placebo. En gruppe fikk også åpen behandling med Entyvio®.
Vedlikeholdsbehandling
Pasienter både fra åpen og blindet induksjonsbehandling, med respons i uke 6, ble randomisert til blindet vedlikeholdsbehandling med Entyvio® hver åttende eller hver fjerde uke, eller placebo. De som ikke oppnådde respons ved uke 6 fikk vedlikeholdsbehandling med Entyvio® åpent hver fjerde uke.
Pasienter med ulcerøs kolitt i GEMINI I1,2
I Gemini I (n = 895) ble effekt og sikkerhet av Entyvio® undersøkt ved behandling av pasienter med moderat til alvorlig aktiv ulcerøs kolitt.
Induksjonsbehandling GEMINI I
I GEMINI I ble 374 pasienter randomisert til å få blindet behandling med Entyvio® (n = 225) eller placebo (n =149). I tillegg fikk 521 pasienter åpen behandling med Entyvio®
Vedlikeholdsbehandling GEMINI I
Pasienter med klinisk respons på Entyvio® (n=373) i uke 6 ble videre randomisert til blindet vedlikeholdsbehandling med Entyvio® hver 4. eller 8. uke eller placebo.
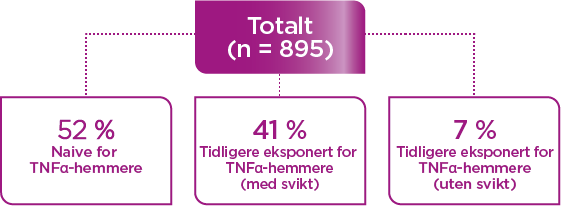
Pasienter sviktet på minst én behandling
Pasienter inkludert i Gemini I var både pasienter som ikke hadde blitt tidligere eksponert for TNFα-hemmere (naive) og pasienter som tidligere hadde blitt eksponert for TNFα-hemmere. Pasienter i Gemini I hadde hatt minst én sviktende konvensjonell behandling (som kortikosteroider og/eller immunmodulatorer) og/eller TNFα-hemmer for ulcerøs kolitt.
Dosering i studien og kombinasjon med andre legemidler
Pasientene ble behandlet med 300 mg Entyvio® hver 4. eller 8. uke. Samtidig stabile doser av 5-ASA, orale kortikosteroider og immunomodulatorer var tillatt.1,2
For mer informasjon se www.felleskatalogen.no.
Effektdata uke 6 og 52 (GEMINI I)1,2
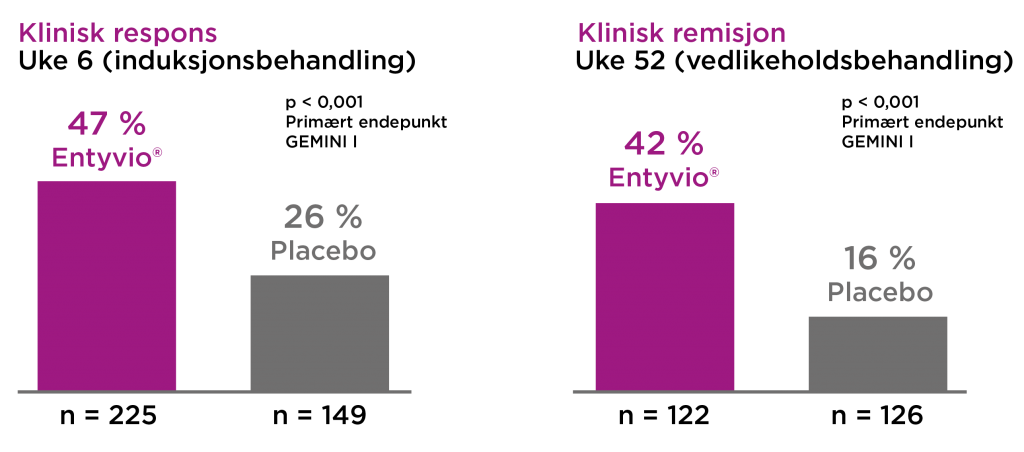
I Gemini I (n = 895) ble effekt og sikkerhet av Entyvio® undersøkt ved behandling av pasienter med moderat til alvorlig aktiv ulcerøs kolitt. Primære endepunkter var klinisk respons ved uke 6 og klinisk remisjon i uke 52. En signifikant høyere andel pasienter oppnådde klinisk respons i uke 6 og klinisk remisjon i uke 52 med Entyvio® hver åttende uke sammenlignet med placebo.
Sekundære endepunkter
- Slimhinnetilheling hos mer enn halvparten av pasientene
Mer enn halvparten (52 %) av pasientene som fikk Entyvio® hver åttende uke oppnådde slimhinnetilheling i uke 52. Dette var signifikant mer enn placebo (20 %). (p<0,001). - Steroidfri remisjon i uke 52
Mer enn dobbelt så mange av pasientene som sto på steroider ved studiestart og som fikk Entyvio® (31 %; n = 70) oppnådde steroidfri remisjon i uke 52 sammenlignet med placebo (14 %; n = 72) (p=0,01).
For mer informasjon, se www.felleskatalogen.no
Definisjoner
- Klinisk respons: En reduksjon av total Mayo score med minst 3 poeng og minst 30 % reduksjon fra utgangspunktet (baseline), med en reduksjon av subscore for rektal blødning med minst 1 poeng eller en absolutt subscore for rektal blødning på 0 eller 1.
- Klinisk remisjon: Mayo score ≤ 2 og ingen subscore >1.
- Slimhinnetilheling: Mayo endoskopisk subscore på 0 eller 1.
- Steroidfri remisjon: Pasienter som brukte perorale kortikosteroider ved utgangspunktet (baseline) og som startet kortikosteroidnedtrapping i uke 6 og var i klinisk remisjon uten steroider i uke 52.
Referanser
- Feagan BG, Rutgeerts P, Sands BE et al. Vedolizumab as induction and maintenance therapy for ulcerative colitis. The New England Journal of Medicine. 2013;369(8):699–710.
- Entyvio® SPC (sist godkjent 20.02.2019), avsnitt 5.1. www.legemiddelsok.no